Key Takeaways
- Luật ‘Quyền Được Thử’ đang được nới lỏng ở Mỹ, gây ra tranh cãi về an toàn và đạo đức y khoa.
- Bang Montana đi đầu trong việc nới lỏng quy định, cho phép cả người không mắc bệnh nghiêm trọng tiếp cận thuốc thử nghiệm.
- Luật ‘Quyền Được Thử’ bỏ qua quy trình phê duyệt nghiêm ngặt của FDA, tiềm ẩn rủi ro về hiệu quả và an toàn thuốc.
- Xu hướng ‘Quyền Được Thử 2.0’ mở rộng sang các bang khác, cho phép điều trị cá nhân hóa dựa trên hồ sơ di truyền.
- Vấn đề tự chủ y tế và an toàn cộng đồng là những yếu tố quan trọng trong cuộc tranh luận về luật ‘Quyền Được Thử’.
Luật ‘Quyền Được Thử’ đang được nới lỏng tại Mỹ, mở ra hy vọng cho nhiều bệnh nhân nhưng cũng đặt ra những câu hỏi lớn về an toàn và đạo đức y khoa. Một hội nghị tại Washington, DC, quy tụ các nhà khoa học, nhà hoạch định chính sách và những người ủng hộ kéo dài tuổi thọ đã làm nóng lên cuộc tranh luận về việc liệu có nên cho phép người dân dễ dàng tiếp cận các loại thuốc thử nghiệm hay không.
Nguồn Cơn Tranh Cãi: Từ “Quyền Được Thử” Đến Nới Lỏng Quy Định
Câu chuyện bắt đầu từ mong muốn đẩy nhanh quá trình phát triển các loại thuốc và phương pháp điều trị nhằm kéo dài tuổi thọ con người. Một trong những hướng tiếp cận được đề xuất là nới lỏng rào cản, cho phép mọi người thử nghiệm các loại thuốc tiềm năng. Lập luận này dựa trên quyền tự do cá nhân, một giá trị được hiến pháp bang Montana đặc biệt đề cao.
Vài năm trước, một nhóm vận động hành lang vì tuổi thọ đã góp phần xây dựng một dự luật mở rộng luật “Right to Try” (Quyền Được Thử) hiện có của bang. Luật ban đầu cho phép những người bệnh nặng nộp đơn xin tiếp cận thuốc thử nghiệm (tức là thuốc chưa được cơ quan quản lý dược phẩm phê duyệt). Bản mở rộng, được thông qua vào năm 2023, đã mở cửa cho cả những người không mắc bệnh nghiêm trọng.

Động thái này không dừng lại ở đó. Vài tháng qua, nhóm vận động tiếp tục thúc đẩy một dự luật mới, quy định chi tiết cách các phòng khám có thể bán các phương pháp điều trị thử nghiệm, chưa được chứng minh cho bất kỳ ai có nhu cầu tại bang. Thông tin về việc dự luật này được thông qua đã lan truyền nhanh chóng, dù văn phòng thống đốc Greg Gianforte ban đầu chưa xác nhận chính thức việc ký thành luật.
Montana Tiên Phong: “Miền Đất Hứa” Cho Thuốc Thử Nghiệm Và Những Dấu Hỏi Lớn
Với việc thông qua dự luật mới, Montana có thể trở thành một trung tâm của Hoa Kỳ cho các phương pháp điều trị thử nghiệm. Tuy nhiên, đây chỉ là một phần của một xu hướng rộng lớn hơn: sự lan rộng của luật “Quyền Được Thử” trên khắp nước Mỹ. Điều này cũng đồng nghĩa với một sự chuyển hướng tiềm ẩn nguy hiểm khỏi y học dựa trên bằng chứng.
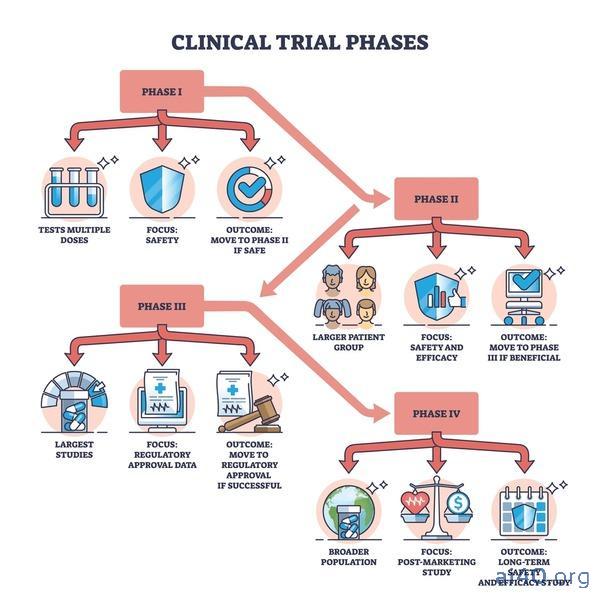
Quy Trình Phê Duyệt Thuốc Nghiêm Ngặt Tại Mỹ
Tại Hoa Kỳ, các loại thuốc phải được thử nghiệm trên người tình nguyện trước khi được phê duyệt và bán ra thị trường. Các thử nghiệm lâm sàng giai đoạn đầu thường có quy mô nhỏ và chủ yếu kiểm tra tính an toàn. Các thử nghiệm giai đoạn sau sẽ đánh giá cả tính an toàn và hiệu quả của một loại thuốc mới.
Hệ thống này được thiết kế để bảo vệ người dân và ngăn chặn các nhà sản xuất bán những sản phẩm không hiệu quả hoặc nguy hiểm – nói cách khác là bảo vệ chúng ta khỏi “thuốc rắn” (snake oil).
Nhu Cầu Tiếp Cận Thuốc Thử Nghiệm
Tuy nhiên, những người mắc bệnh hiểm nghèo và đã cạn kiệt các lựa chọn điều trị khác thường tuyệt vọng muốn thử các loại thuốc thử nghiệm. Họ coi đó là tia hy vọng cuối cùng. Đôi khi họ có thể tình nguyện tham gia các thử nghiệm lâm sàng, nhưng thời gian, khoảng cách và các tiêu chí đủ điều kiện có thể loại trừ lựa chọn đó.
Từ những năm 1980, những người bệnh nặng hoặc giai đoạn cuối không thể tham gia thử nghiệm vì một lý do nào đó có thể nộp đơn xin tiếp cận các phương pháp điều trị thử nghiệm thông qua chương trình “sử dụng nhân đạo” (compassionate use) do Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) điều hành. FDA phê duyệt gần như tất cả các yêu cầu sử dụng nhân đạo mà họ nhận được, mặc dù các nhà sản xuất không phải lúc nào cũng đồng ý cung cấp thuốc của họ vì nhiều lý do.
Sự Ra Đời Và Lan Rộng Của Luật “Quyền Được Thử”
Điều này vẫn chưa đủ đối với Goldwater Institute, một tổ chức theo chủ nghĩa tự do, đã soạn thảo luật “Quyền Được Thử” mẫu vào năm 2014 cho những người mắc bệnh nan y. Các phiên bản của dự thảo này sau đó đã được thông qua thành luật ở 41 tiểu bang của Hoa Kỳ, và Hoa Kỳ đã có luật “Quyền Được Thử” liên bang từ năm 2018. Các luật này thường cho phép những người bệnh nặng nộp đơn xin tiếp cận các loại thuốc mới chỉ qua các giai đoạn thử nghiệm lâm sàng rất sớm (thường là Giai đoạn I, có thể chỉ được thử nghiệm trên khoảng 20 người khỏe mạnh), miễn là họ đưa ra sự đồng ý éclairé (informed consent).
Nhiều người cho rằng các luật này được thúc đẩy bởi sự không hài lòng với cả quy định về thuốc và FDA. Xét cho cùng, chúng được thiết kế để đạt được kết quả tương tự như chương trình sử dụng nhân đạo, điểm khác biệt duy nhất là chúng bỏ qua FDA. Điều đáng lưu ý là các phương pháp điều trị này đang ở giai đoạn rất sớm. Một loại thuốc đã qua thử nghiệm Giai đoạn I có thể mới chỉ được thử nghiệm trên một số ít người khỏe mạnh. Mặc dù các thử nghiệm này được thiết kế để kiểm tra tính an toàn, chúng không bao giờ là kết luận cuối cùng. Ở giai đoạn đó, không ai có thể biết một người bệnh – người có khả năng đang dùng các loại thuốc khác – sẽ phản ứng với nó như thế nào.
“Quyền Được Thử 2.0”: Làn Sóng Mở Rộng Và Nguy Cơ Tiềm Ẩn
Giờ đây, các luật “Quyền Được Thử” này đang được mở rộng hơn nữa. Dự luật của Montana, đi xa nhất, sẽ cho phép những người không mắc bệnh nghiêm trọng tiếp cận các phương pháp điều trị chưa được chứng minh. Các tiểu bang khác cũng đang có những động thái tương tự.
Mới đây, thống đốc bang Georgia đã ký thành luật Hope for Georgia Patients Act (Đạo luật Hy vọng cho Bệnh nhân Georgia), cho phép những người mắc bệnh đe dọa tính mạng tiếp cận các phương pháp điều trị được cá nhân hóa, tức là “duy nhất và được sản xuất riêng cho một bệnh nhân dựa trên hồ sơ di truyền của chính họ”. Các luật tương tự, được gọi là “Right to Try 2.0” (Quyền Được Thử 2.0), cũng đã được thông qua ở các tiểu bang khác, bao gồm Arizona, Mississippi, và North Carolina.
Năm ngoái, bang Utah đã thông qua một đạo luật cho phép các nhà cung cấp dịch vụ chăm sóc sức khỏe (bao gồm cả bác sĩ chỉnh hình, bác sĩ chuyên khoa chân, nữ hộ sinh và bác sĩ tự nhiên liệu pháp) cung cấp các liệu pháp tế bào gốc từ nhau thai chưa được phê duyệt. Các phương pháp điều trị này liên quan đến các tế bào được thu thập từ nhau thai, được cho là có hứa hẹn trong việc tái tạo mô. Tuy nhiên, chúng chưa được thử nghiệm trên người, có thể tốn hàng chục nghìn đô la và tác dụng của chúng vẫn chưa được biết rõ. Luật của Utah được một luật sư chuyên về luật FDA mô tả là “một thách thức khá trắng trợn đối với thẩm quyền của FDA“, và là một điều có thể gây nguy hiểm cho bệnh nhân.
Tiếng Nói Trái Chiều: Giữa Quyền Tự Quyết Y Tế Và An Toàn Cộng Đồng
Những đạo luật như thế này làm dấy lên nhiều cuộc tranh luận rất nhạy cảm. Một số người cho rằng đó là vấn đề tự chủ y tế, và mọi người nên có quyền lựa chọn những gì họ đưa vào cơ thể mình.
Nhiều người khác lại lập luận rằng cần phải tính toán chi phí-lợi ích. Một người bệnh nặng có khả năng thu được nhiều lợi ích hơn và ít mất mát hơn khi thử một loại thuốc thử nghiệm, so với một người khỏe mạnh.
Tuy nhiên, tất cả mọi người đều cần được bảo vệ khỏi các loại thuốc không hiệu quả. Hầu hết các nhà đạo đức học cho rằng việc bán một phương pháp điều trị khi bạn không biết liệu nó có tác dụng hay không là phi đạo đức, và lập luận này đã được nhiều quyết định của tòa án Hoa Kỳ ủng hộ trong nhiều năm qua.
Cũng có thể có động cơ tài chính để các bác sĩ đề xuất một loại thuốc thử nghiệm, đặc biệt là khi họ được pháp luật bảo vệ (luật “Quyền Được Thử” có xu hướng bảo vệ các bác sĩ kê đơn khỏi các hành động kỷ luật và kiện tụng nếu có sự cố xảy ra).
Trên hết, nhiều nhà đạo đức học cũng lo ngại rằng quy trình phê duyệt thuốc của chính FDA đã suy giảm trong khoảng một thập kỷ qua. Họ cho rằng ngày càng có nhiều loại thuốc được phê duyệt nhanh chóng dựa trên bằng chứng yếu.
Kết luận
Cuộc tranh luận về việc mở rộng luật “Quyền Được Thử” tại Mỹ phản ánh một sự giằng co phức tạp giữa khao khát chữa bệnh, quyền tự quyết của bệnh nhân và sự cần thiết phải đảm bảo an toàn dựa trên bằng chứng khoa học. Trong khi một số người coi đây là cơ hội mang lại hy vọng, những người khác lại cảnh báo về những rủi ro tiềm ẩn khi bỏ qua các quy trình đánh giá nghiêm ngặt của FDA. Các nhà khoa học và đạo đức học ở cả hai phía đang chờ xem điều gì sẽ xảy ra dưới chính quyền mới của Hoa Kỳ. Như lời của Diana Zuckerman, chủ tịch Trung tâm Nghiên cứu Sức khỏe Quốc gia phi lợi nhuận: “Đôi khi hy vọng giúp mọi người làm tốt hơn. Nhưng trong y học, liệu có tốt hơn không khi hy vọng dựa trên bằng chứng thay vì hy vọng dựa trên sự thổi phồng?” Câu hỏi này vẫn còn bỏ ngỏ, đòi hỏi sự cân nhắc kỹ lưỡng từ các nhà hoạch định chính sách và cộng đồng y khoa.